XIXe Siècle
1800 -> La pile Volta (pile voltaïque) : Elle a été inventée par Alessandro Volta, un physicien italien. Il était connu pour ses travaux sur l'électricité et pour l'invention de la première pile électrique. La pile Volta est formée par un empilement, d'où son nom, de petits disques de cuivre et de zinc alternés. Chaque disque de cuivre est séparé du disque de zinc du dessous par une surface de tissu ou de feutre imbibé de saumure, solution aqueuse de Chlorure de sodium, alors que le disque de cuivre suivant est en contact direct avec le disque de zinc du dessus. De cette façon, on a un empilement : cuivre, saumure, zinc, cuivre, saumure, zinc, etc. Il se produit au niveau de chaque couche, qu'on appellera désormais une superposition d'un disque de cuivre et d'un disque de zinc, séparés par un tissu retenant la solution, une réaction d’oxydo-réduction. Il ne se passe rien au niveau du disque de cuivre. Les éléments participant à l'oxydation et à la réduction sont les éléments zinc et eau. La mise en série de couches permet d’obtenir une tension électrique plus élevée.

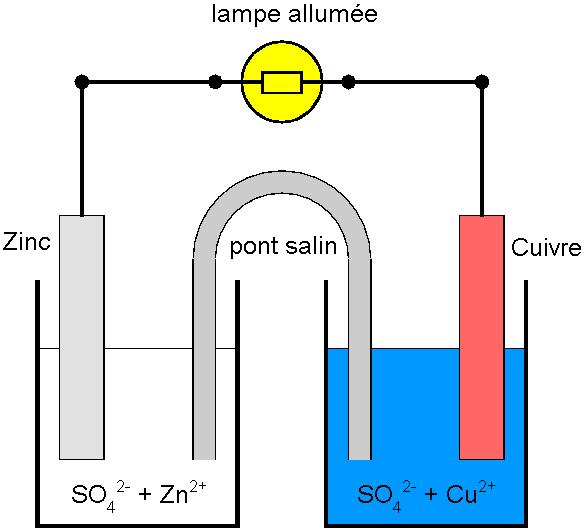
1836 -> La pile Daniell : Elle a été inventée par le chimiste britannique John Daniell en 1836 au moment où le développement du télégraphe faisait apparaître un besoin urgent de sources de courant sûres et constantes. La pile de Daniell est une pile dans laquelle s'effectue une réaction d'oxydo-réduction, dont l'échange d'électrons entre le zinc, servant d'anode, et le cuivre, servant de cathode, est à l'origine du courant électrique. La pile est constituée de deux compartiments dont l'un contient une solution de sulfate de zinc dans laquelle est immergée une plaque de zinc métallique. L'autre compartiment de la pile contient une solution de sulfate de cuivre dans laquelle baigne une plaque métallique de cuivre. Les deux solutions sont reliées par un pont satin appelé aussi pont électrolytique (solution de chlorure de potassium) qui sert à équilibrer les charges.
1859 -> L’accumulateur au plomb : Il a été inventé par Gaston Planté qui était un physicien et inventeur français. Il est principalement connu pour l'invention de l'accumulateur électrique (batterie au plomb). Dans un accumulateur au plomb chargé, l’électrode positive est formée d’une couche d’oxyde de plomb solide déposée sur une grille d’alliage de plomb et l’électrode négative est formée d’une couche de plomb déposée sur une grille d’alliage de plomb. Ces deux grilles de plomb, roulées en spirales et séparées par une toile de lin, sont plongées dans un bac contenant l’électrolyte. L’électrolyte est une solution aqueuse d’acide sulfurique. Contrairement à ce qui se passe dans la plupart des types d’accumulateurs, l’électrolyte participe aux réactions de charge et de décharge et l’évolution de la concentration de l’acide sulfurique lors de la charge et de la décharge. Ces accumulateurs étaient associés en batterie.
à l'époque de Gaston Planté :

De nos jours :

1867 -> La pile Leclanché (pile saline) : Elle a été inventée par Georges Leclanché qui était un ingénieur français. Au pôle négatif de la pile, l'électrode de zinc est au contact d'une solution gélifiée de chlorure de zinc, et de chlorure d’ammonium. Au pôle positif de la pile, l'électrode en graphite est entourée d'un mélange de dioxyde de manganèse et de carbone en poudre. Ce mélange est imbibé de la solution gélifiée de chlorure d'ammonium. Le carbone est un conducteur qui permet aux électrons qui arrivent à l'électrode de graphite de réduire le dioxyde de manganèse dans la masse du mélange et de l'utiliser en totalité. Ceci permet de fournir une tension électrique. De nos jours, cette pile est toujours utilisée (avec des améliorations).

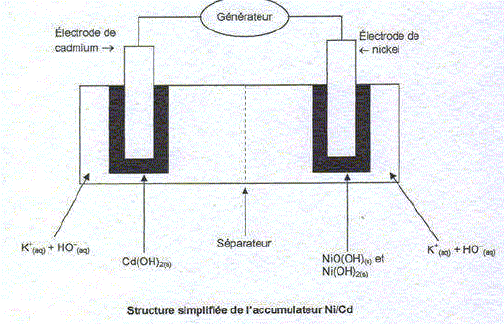
1899 -> L’accumulateur nickel-cadmium : il a été inventé par Waldemar Jungner qui était un ingénieur suédois. Dans un accumulateur nickel-cadmium chargé, l’électrode positive est constituée d’oxo hydroxyde de nickel et de graphite de l’électrode négative est un cadmium. L’électrolyte est une solution aqueuse concentrée d’hydroxyde de potassium. L’électrolyte participe aux réactions de décharge et de charge, mais sa concentration ne change pas.